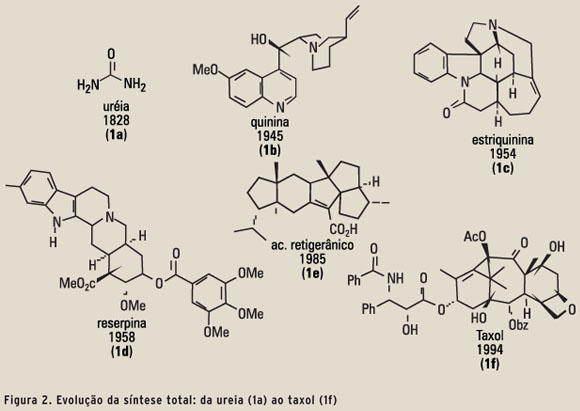

A evolução da química orgânica sintética. Quo vadis?
Carlos Roque Duarte Correia
Caio C. Oliveira
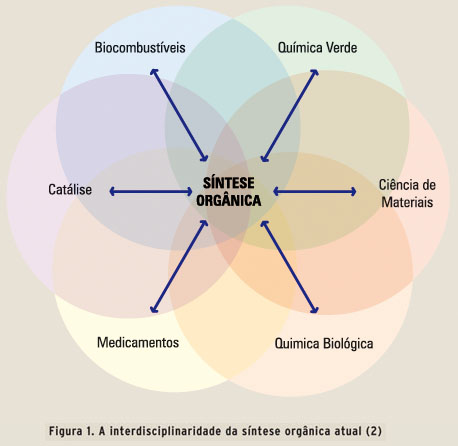
A síntese orgânica é uma ciência em constante evolução. Até a década de 1950, as atividades do químico orgânico sintético eram basicamente: 1. elucidação estrutural de produtos naturais; 2. investigação de reações básicas; e 3. preparação de novas substâncias químicas. Após esse período, além da manutenção das atividades acima – que foram aperfeiçoadas e simplificadas com o surgimento de técnicas modernas como a ressonância magnética nuclear e a espectrometria de massas –, a sua forte associação atual com a biologia, a medicina e as ciências ambientais e de materiais conferiu à síntese orgânica um caráter ainda mais dinâmico e interdisciplinar.(1)
Além disso, o desenvolvimento de novas reações orgânicas, ainda mais robustas e estereosseletivas (3), tornou a síntese de moléculas cada vez mais complexas uma realidade. Historicamente, a química orgânica e a síntese orgânica (atividades científicas siamesas), tiveram sua origem na preparação em laboratório de uma substância natural contendo apenas um átomo de carbono, a ureia (1a), sintetizada por Wöhler em 1828 (4). A evolução para as sínteses atuais envolvendo moléculas com acentuada complexidade estrutural, tal como o taxol (1f) – sintetizado por Holton e Nicolaou em 1994 (5) –, é decorrente do desenvolvimento de novas técnicas de laboratório, novas metodologias de síntese, mais seletivas e robustas e, também, em grande medida, pelo amadurecimento da "filosofia" adotada para a execução de um empreendimento sintético, como por exemplo, o planejamento estratégico a ser seguido.
]]>

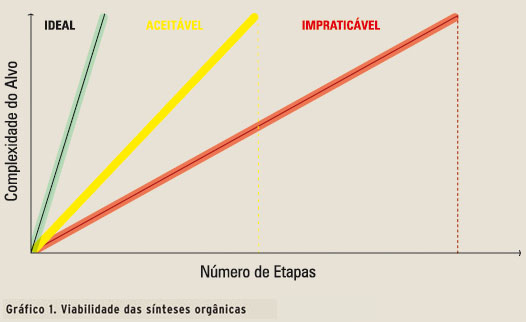
Com o fortalecimento do conceito de química verde a partir de 1990, a pressão da sociedade pelo desenvolvimento de processos sustentáveis promoveu uma mudança no paradigma da síntese orgânica. Em 1992, Carlson propôs o conceito de reação ideal, envolvendo o uso de água como solvente, materiais de partida de fácil acesso, baratos, não-tóxicos e a obtenção do produto de maneira fácil, em rendimento quantitativo (6). Complementarmente, Wender afirma que o número de etapas é outro fator de grande influência na viabilidade de uma síntese, pois determina tempo, custo, quantidade de resíduos e escala do processo (Gráfico 1) (7). Mas como fazer isto?
]]> Para se realizar a síntese de uma substância (ou molécula) com elevada complexidade estrutural, é necessário utilizar metodologias que promovam as transformações desejadas de maneira controlada (estéreo e quimiosseletiva) (8) e, se possível, com a formação sequencial de mais de uma ligação química. Assim, a geração de resíduos é reduzida em função de um número menor de etapas. Nesse cenário, as reações catalíticas surgem como uma ferramenta importante nessa nova era da síntese orgânica. As recentes premiações do Prêmio Nobel de Química, diretamente relacionadas ao desenvolvimento de métodos catalíticos em química orgânica, são um claro reflexo da importância desse tipo de reações: 1. William S. Knowles, R. Noyori e K. Barry Sharpless, em 2001, pelas reações catalíticas enantiosseletivas; 2. Yves Chauvin, Robert Grubbs e Richard Schrock, em 2005, pelas reações de metátese de olefinas; e 3. Richard F. Heck, Ei-ichi Negishi e Akira Suzuki, pelas reações de cross-coupling catalisadas por paládio, em 2010 (9).
NOVAS FERRAMENTAS SINTÉTICAS O ressurgimento da organocatálise (reações catalíticas promovidas por uma molécula orgânica), no final da década de 1990, mostrou-se uma alternativa valiosa no desenvolvimento de novas ferramentas sintéticas (10). Esse método de catálise foi inspirado na atuação das enzimas, visando favorecer a formação de moléculas de forma enantiosseletiva (que favorece a formação de um dos enantiômeros). A receptividade da comunidade sintética com a organocatálise pode ser avaliada pelo grande número de publicações sobre o tema entre os anos de 2000 e 2010.
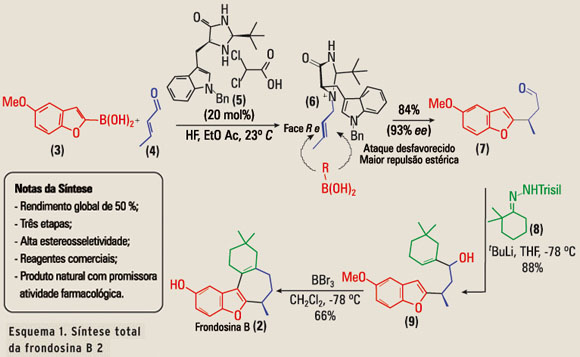
A síntese total do sesquiterpeno de origem marinha frondosina B 2, relatada por MacMillan em 2010, ilustra bem a importância da descoberta de novas reações e como a aplicação deste conhecimento promove um acesso rápido a moléculas de interesse medicinal (11). Esse terpeno apresenta alto potencial anti-inflamatório e antineoplásico in vitro. Por esse motivo, desde o seu isolamento em 1997 da esponja marinha Dysidea frondosa (12), três outras sínteses totais já foram relatadas, sendo que a mais eficiente delas foi relatada por Ovaska, em 2009, envolvendo uma rota com 10 etapas e 13% de rendimento global (13). A abordagem de MacMillan partiu da adição enantiosseletiva (14) do ácido borônico 3 ao crotonaldeído 4 catalisada pela imidazolidinona 5 em 84% de rendimento e elevado excesso de um dos enantiômeros (razão de 97:03). O produto natural foi obtido após mais duas etapas: reação do aldeído 7 com a arilsulfinil-hidrazona 8 (reação de Shapiro); e um processo de desmetilação, ciclização intramolecular (reação de Friedel-Crafts) e isomerização de uma ligação dupla, em uma única etapa, no mesmo frasco reacional (one-pot). (Esquema 1).
Dentre as ferramentas utilizadas pelos químicos orgânicos sintéticos para obter um rápido aumento na complexidade de produtos desejados, destacam-se as reações sequenciais do tipo dominó, caracterizadas pela formação de duas ou mais ligações C-C, C-O ou C-N na molécula alvo, sem que haja isolamento de intermediários ou adição de outro reagente. A transformação subsequente decorre da funcionalização ocorrida anteriormente (15). Dessa forma, reduzem-se as etapas de isolamento e purificação e o número de passos reacionais, além de se promover uma sensível diminuição na geração de resíduos e no custo total do processo. Para se entender como a economia de etapas é importante numa rota de síntese, considere-se um material de partida (MP) e um produto (P) com massa molar igual a 500 g/ mol. Supondo a transformação de 1 mol do MP no respectivo P, em 5 etapas, com rendimento médio de 90%, a massa de P, ao final da síntese, será de 295 g (59% de rendimento global). Contudo, se o número de etapas aumentar para 15, mantendo-se um rendimento médio de 90%, serão obtidos somente 103 g do produto P (21% de rendimento global) (1). Mesmo considerando-se rendimentos excepcionais de 90% em todas as etapas, a perda de massa é um problema inerente a uma rota linear muito longa. Sobre esta questão, Tietze comentou em 2004 que rotas sintéticas com mais de 20 etapas devem ser evitadas, por não serem econômicas – e ecologicamente justificáveis (16).
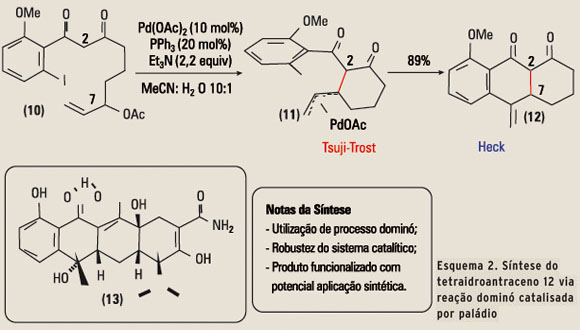
A síntese do tetraidroantraceno 12 em um único passo reacional, via um processo dominó envolvendo o uso de paládio catalítico, foi relatada por Tietze em 2001 (Esquema 2) (17). A transformação envolveu duas reações intramoleculares possuindo nomes próprios: uma reação de Tsuji-Trost seguida de uma reação de Heck. A formação das duas ligações C-C chaves, empregando-se o mesmo sistema catalítico, ilustra não apenas a engenhosidade do método como também a versatilidade da catálise por paládio, promovendo reações consecutivas, via mecanismos distintos, de forma eficiente (89% de rendimento). Esta mesma estratégia sintética foi aplicada posteriormente na síntese de análogos do antibiótico tetraciclina 13 (18).
]]>
O desenvolvimento da síntese orgânica nos últimos 60 anos foi notável, e isso se deve, em grande parte, ao surgimento de métodos analíticos mais precisos (RMN e 1H e 13C, espectrometria de massas, novos métodos de separação cromatográfica etc), ao planejamento estratégico racional das rotas e, não menos importante, ao poder das novas metodologias sintéticas. Dessa maneira, feitos notáveis foram realizados, como a síntese de moléculas de grande complexidade estrutural com o taxol (1f), palitoxina (19) e a brevetoxina (20). Valendo-se da lógica, criatividade, perseverança e tecnologias disponíveis, a síntese de um número incontável de produtos naturais, ou mesmo não naturais, estão hoje ao alcance no laboratório. A síntese de moléculas complexas representa um terreno fértil para testes do potencial de uma nova metodologia sintética (viabilidade, versatilidade. robustez e impacto ambiental), assim como proporciona um desafio intelectual de alto nível e um excepcional treinamento para estudantes de pós-graduação.
A síntese orgânica tem se adaptado às novas exigências da sociedade e da comunidade científica. Por exemplo, atuam hoje de forma conjunta as sínteses alvo-orientadas (síntese de uma molécula específica, comumente um produto natural bioativo) e as abordagens de síntese função-orientada (síntese de moléculas, ou um conjunto delas, de maneira a alcançar uma atividade específica). Esse último método é largamente utilizado no descobrimento de novos fármacos, daí a tendência atual e futura de uma interação cada vez maior entre a síntese orgânica, a química medicinal, a farmacologia, a biologia e a bioquímica, exigindo uma boa formação dos futuros químicos nessas áreas da ciência. Além disso, a química orgânica é e continuará sendo uma ferramenta fundamental no desenvolvimento de biocombustíveis (21), novos materiais (ex. dendrímeros) (22) e na agregação de valor a materiais derivados da biomassa (ex. gliceroquímica) (Esquema 3) (23).
O trabalho em síntese orgânica, essencialmente experimental, é árduo e exigente no que diz respeito a empenho, habilidades em laboratório e perseverança, qualidades essas essenciais para se alcançar bons resultados. É esta busca interminável por conhecimento e novas fronteiras que a torna uma ciência fascinante e capaz de grandes realizações para aqueles que se dedicarem a ela com empenho e criatividade.
Carlos Roque Duarte Correia é professor titular do Instituto de Química da Universidade Estadual de Campinas (Unicamp). Atua na área de síntese orgânica, tendo como foco a síntese de compostos bioativos via reações de acoplamentos cruzados mediados por paládio, empregando principalmente sais de arenodiazônio.
Caio C. Oliveira é doutorando do Instituto de Química da Unicamp.
NOTAS E REFERÊNCIAS BIBLIOGRÁFICAS
]]>1. T. Hudlický, J. Reed, The way of synthesis, (Wiley-VCH, Weinheim, 2007), pp. 3-128.
2. Os autores agradecem a colaboração do prof. Paulo C. M. L. Miranda (Instituo de Química/ Unicamp) na confecção dessa figura.
3. Reação estereosseletiva: reação na qual um dos possíveis estereoisômeros é formado mais rapidamente do que o(s) outro(s), assim, este é produzido em maior proporção no meio reacional.
4. Friedrich Wöhler.Ueber künstliche bildung des harnstoffs. Ann. der Physik, Ann, 88, 253-256 (1828).
5. Holton, Robert A.; Somoza, Carmen; Kim, Hyeong Baik; et all. "First total synthesis of taxol. 1. Functionalization of the B Ring." J . Am. Chem. Soc. 116, 1597-1598 (1994). Nicolaou, K.C. Z.; Yang, J.J. et all. "Total synthesis of taxol". Nature, 367, 630–634 (1994).
6. Carlson, Rolf; Carlson, Johan. Desing and optimization in organic synthesis. Elsevier, Amsterdam, 2005, vol. 24, cap. 1.
7. Wender, Paul A.; Verma,Vishal A.; Paxton, Thomas J.; Pillow, Thomas H.. "Function-oriented synthesis, step economy, and drug design". Acc. Chem. Res. 41, 40-49 (2008).
8. Reação quimiosseletiva: reação na qual a transformação ocorre seletivamente em um grupo funcional em detrimento dos outros presentes na molécula em estudo.
9. Nobel Prize website. http//www.nobelprize.org, acessado em abril de 2010.
10. Berkessel, A.; Gröger, H.. Asymmetric organocatalysis: from biomimetic concepts to applications in asymmetric synthesis. Wiley-VCH, Weinheim, 2005, pp. 1-8.
11. MacMillan, David W. C.; Reiter, Maud; Torssell, Staffan; Lee, Sandra. "The organocatalytic three-step total synthesis of (+)-frondosin B", Chem. Sci. 1, 37–42 (2010).
12. Patil, Ashok D.; Freyer, Alan J. et all. "Five new sesquiterpene hydroquinone derivatives with novel skeletons from the sponge Dysidea frondosa: inhibitors of interleukin-8 receptors". Tetrahedron, 53, 5047–5060 (1997).
13. Ovaska, Timo V.; Sullivan, Jonathan A.; et all. "Asymmetric synthesis of seven-membered carbocyclic rings via a sequential oxyanionic 5-exo-dig cyclization/claisen rearrangement process. total synthesis of (+)-frondosin B". Org. Lett. 11, 2715–2718 (2009).
14. Reação enantiosseletiva: reação na qual um enantiômero é formado mais rapidamente do que o outro; assim, este é formado em maior proporção no meio reacional.
15. Tietze, L. F.; Brasche, G.; Gericke K. M.. Domino reactions in organic synthesis, Wiley-VCH, Weinheim, 2006, pp. 1-10.
16. Tietze, Lutz. F.; Rackelmann, Nils. "Domino reactions in the synthesis of heterocyclic natural products and analogs". Pure Appl. Chem. 76, 1967-1983 (2004).
17. Tietze, Lutz F.; Nordmann, Gero. "A novel palladium-catalyzed domino-tsuji-trost-process for the synthesis of tetrahydroanthracenes". Eur. J. Org. Chem. pp. 3247-3253. 2001.
]]>18. Tietze, Lutz F.; Redert, Thomas; et all. "Efficient synthesis of the structural core of tetracyclines by a palladium-catalyzed domino tsuji– trost–heck–mizoroki reaction". Chem. Eur. J. 14, 2527-2535 (2008).
19. Kishi, Yoshito; Armstrong, Robert W. et all. "Total synthesis of a fully protected palytoxin carboxylic acid". J. Am. Chem. Soc. 111, 7525– 7530 (1989).
20. Nicolaou, K. C.; Theodorakis, E. A.; et all. "Total synthesis of brevetoxin b. 2. completion". J. Am. Chem. Soc. 117,1173–1174 (1995).
21. Noordermee, Minke A.; Petrus, Leo. "Biomass to biofuels, a chemical perspective". Green Chem. 8, 861-867 (2006).
22. Estroff, Lara A.; Hamilton, Andrew D.. "At the interface of organic and inorganic chemistry: bioinspired synthesis of composite materials". Chem. Mater. 13, 3227–3235 (2001).
]]>23. Corma, Avelino; Iborra, Sara; Velty, Alexandra. "Chemical routes for the transformation of biomass into chemicals". Chem. Rev. 107, 2411– 2502 (2007).
24. Zhang, Xiaojun; Luo, Rongcong; et all. "Application of (R)-3-hydroxyalkanoate methyl esters derived from microbial polyhydroxyalkanoates as novel biofuels". Biomacromolecules, 10, 707–711 (2009).
25. Zimmerman, Steven C.; Quinn, Jordan R.; et all. "Cross-linked glycerol dendrimers and hyperbranched polymers as ionophoric, organic nanoparticles soluble in water and organic solvents". Angew. Che. Int. Ed. 46, 8164- 8167 (2007).
26. Shi, Yan; Dayoub, Wissam; et all. "Straightforward selective synthesis of linear 1-o-alkyl glycerol and di-glycerol monoethers". Tetrahedron Lett. 50, 6891-6893 (2009).cenes". Eur. J. Org. Chem. 3247-3253 (2001).
]]>